Wirksamkeit
HETLIOZ® wurde speziell für die Behandlung von Non-24 bei völlig blinden Erwachsenen entwickelt und in einem umfangreichen Studienprogramm getestet. Eine große Herausforderung war die Patientenrekrutierung für die Phase III-Studien, da die Population der völlig blinden Menschen insgesamt sehr klein ist. Non-24 ist als zyklische zirkadiane Schlaf-Wach-Rhythmusstörung weitgehend unbekannt und bei den meisten Betroffenen nicht diagnostiziert. Die beiden Phase III-Studien umfassen die größte Population völlig blinder Patienten mit Non-24, die je an einer klinischen Studie teilgenommen haben.
Die Herausforderung, sinnvolle klinische Endpunkte bei einer zyklischen Störung zu finden
Eine weitere Herausforderung für die Phase III-Studien war die Definition von klinischen Endpunkten, die die zyklische Natur der Symptome widerspiegeln und auch die unterschiedliche Zykluslänge der einzelnen Patienten berücksichtigen. Solche Endpunkte gab es bisher nicht.
Die zirkadiane Zykluslänge ist definiert als die Zahl der Tage zwischen zwei aufeinanderfolgenden Angleichungen des biologischen Tags mit dem 24-Stundentag. Je nach Länge des biologischen Tages kann die individuelle Zykluslänge Wochen bis Monate umfassen. Die stärksten Symptome treten auf, wenn die innere Nacht auf den äußeren Tag fällt (vermehrte Müdigkeit und Schlafattacken über Tag, schlechter Schlaf in der Nacht, die dann mit dem biologischen Tag zusammenfällt) und die Symptomatik ist am geringsten, wenn die innere Nacht mit der Umgebungsnacht übereinstimmt.1,2
Neben den Gesamtschlafzeiten pro Tag (aufgeteilt in Gesamt-Nachtschlafzeit und Gesamt-Tagesschlafzeit) kommt daher der Symptomatik an den schlechtesten Tagen und Nächten des Zyklus (die wahrscheinlich dem Gegenlauf des biologischen Tages zum Umgebungstag entsprechen) eine besondere Bedeutung für das Erkennen des Ausmaßes der zirkadianen Störung bzw. seiner Verbesserung durch eine Synchronisierung zu. Aus diesem Grund wurden zusätzlich innerhalb des individuellen Zyklus der Patienten die durchschnittliche Gesamt-Nachtschlafzeit an den 25 % der Tage mit dem schlechtesten Schlaf nachts (unteres Quartil der Gesamt-Nachtschlafzeit) und die durchschnittliche Gesamt-Tagesschlafzeit an den 25 % der schlechtesten Tage mit dem meisten Schlaf tagsüber (oberes Quartil der Gesamt-Tagesschlafzeit) separat ausgewertet. Die einzelnen Schlafepisoden nachts und über den Tag wurden von den Patienten täglich detailliert über die gesamte Studienzeit in einem Schlaftagebuch festgehalten. Sie wurden jeweils morgens und abends elektronisch zur Auswertung übermittelt.3
Da Non-24 nicht nur Auswirkungen auf den Schlaf der Patienten hat, sondern auch ihren generellen gesundheitlichen Zustand und ihre Funktionsfähigkeit im sozialen Rahmen beeinflussen kann, wurde die klinische Gesamtfunktion der Patienten in der Clinical Global Impression of Change Skala (CGI-C) im Vergleich zum Zustand vor Therapiebeginn alle zwei Monate vom Studienarzt beurteilt.3
Es wurden zwei randomisierte, multizentrische, doppelblinde, placebokontrollierte Phase III-Studien mit unterschiedlicher Zielsetzung durchgeführt:3
- SET-Studie:3
Synchronisierung des biologischen Tags mit dem 24-Stundentag durch HETLIOZ® bei völlig blinden Erwachsenen mit freilaufendem zirkadianen Rhythmus (Non-24) - RESET-Studie:3
Aufrechterhaltung der Synchronisierung unter Fortführung der Tasimelteon-Behandlung bzw. nach Switch auf Placebo
Primäre Endpunkte waren bei beiden Studien die Synchronisierung der endogenen Periode mit dem 24-Stundentag und das klinische Ansprechen.
Synchronisierung: Die endogene Periode jedes Patienten wurde aufgrund des Rhythmus des Peaks von 6-Sulfatoxymelatonin, des Hauptmetaboliten von Melatonin im Urin, ermittelt.4,5 Für die Einstufung als erfolgreiche Synchronisation des Patienten mit dem 24-Stundentag musste die endogene Periode τ (tau) 24,1 Stunden sein.3
SET-Studie
Signifikant häufigere Synchronisierung und signifikante Symptombesserung durch HETLIOZ® bereits im ersten Behandlungsmonat im Vergleich zu Placebo
Studiendesign3
Randomisierte, doppelblinde, placebokontrollierte, multizentrische Studie an völlig blinden, erwachsenen Patienten mit Non-24 (n=84). 391 Patienten wurden gescreent. Patienten mit einem nicht-synchronisierten zirkadianen Melatonin-Rhythmus (Periode τ (tau) ≥ 24,25 h) und Erfüllung aller weiteren Einschlusskriterien wurden randomisiert auf die Behandlung mit HETLIOZ® 20 mg oder Placebo, 1 Stunde vor der Bettgehzeit, verteilt und 6 Monate behandelt. Die primären Endpunkte (Synchronisierung und klinisches Ansprechen) wurden bereits nach 4-wöchiger Behandlung erhoben, um die Schnelligkeit des Eintritts der Synchronisierung abschätzen zu können. Im Anschluss an die SET-Studie wechselte ein Teil der HETLIOZ®-Patienten in die RESET-Studie. Bei diesen wurde nach 7 Monaten HETLIOZ® Behandlung eine weitere Synchronisationsabschätzung auf Basis der Melatonin-Peaks vorgenommen.
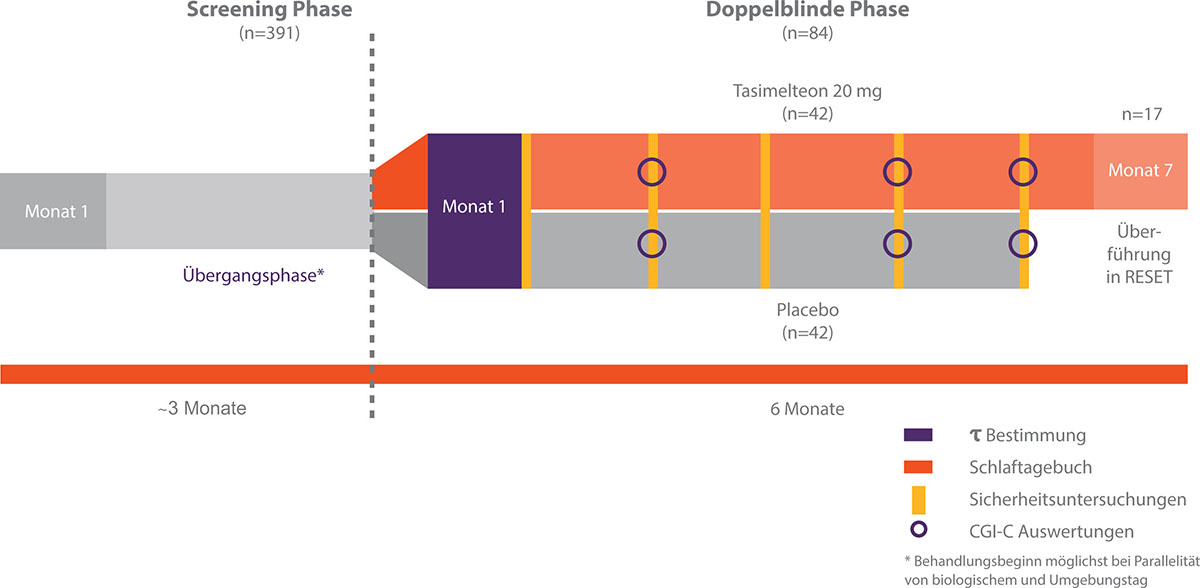
Abbildung 1: Design der SET-Studie3
Ergebnisse der SET-Studie (nach einem Behandlungsmonat):
- Innerhalb des ersten Behandlungsmonats wurden 20 % der HETLIOZ®-Patienten erfolgreich mit dem 24-Stundentag synchronisiert, während eine Synchronisierung in der Placebo-Gruppe nur bei 3 % der Patienten auftrat (p=0,0171).3,6
- 24 % der Patienten sprachen unter HETLIOZ® im zusammengesetzten Endpunkt klinisch an, unter Placebo keiner (p=0,0028).3,6
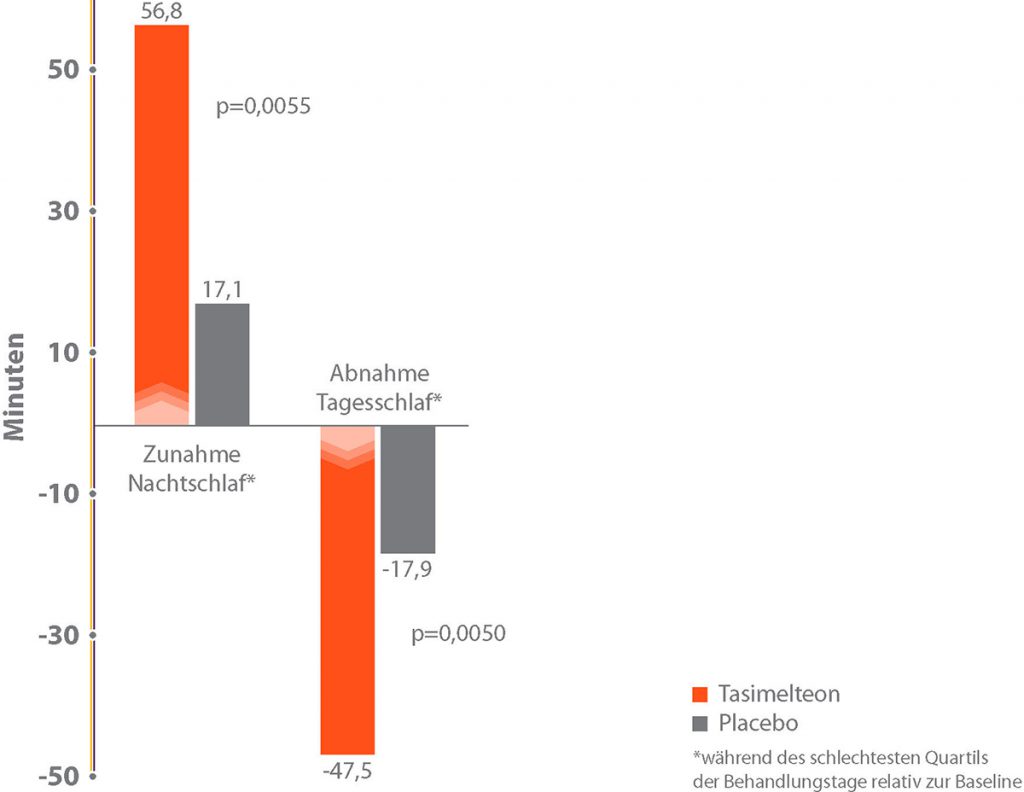
Abbildung 2: SET-Studie: Veränderungen in der Schlafdauer nachts und tagsüber in den 25 % der symptomreichsten Nächte bzw. Tage innerhalb des ersten Behandlungsmonats3
- Der Nachtschlaf während der schlechtesten 25 % der Behandlungstage verbesserte sich im Schnitt bei den HETLIOZ®-Patienten (einschließlich der nicht-synchronisierten) um fast 1 Stunde, unter Placebo nur um 17 Minuten (p=0,0055).3,6
- Umgekehrt nahm der Tag-Schlaf unter HETLIOZ® während der schlechtesten 25 % der Behandlungstage um 46 min ab und unter Placebo nur um 18 min (p=0,0050).3,6
- Die klinische Gesamtbewertung nach der Clinical Global Impression of Change (CGI-C)-Skala
zeigte für HETLIOZ®-Patienten mit dem Wert 2,6 eine klare Verbesserung und für Placebo-Patienten3,4 mit dem Wert 3,4 einen Wert zwischen keiner Veränderung und minimaler Verbesserung (p=0,0093). Der Wert 4 entspricht keiner Veränderung, der Wert 1 einer sehr starken Verbesserung, der Wert 7 einer sehr starken Verschlechterung.6 Die CGI-C-Skala reflektiert die generelle soziale, berufliche und gesundheitliche Funktionalität der Patienten.
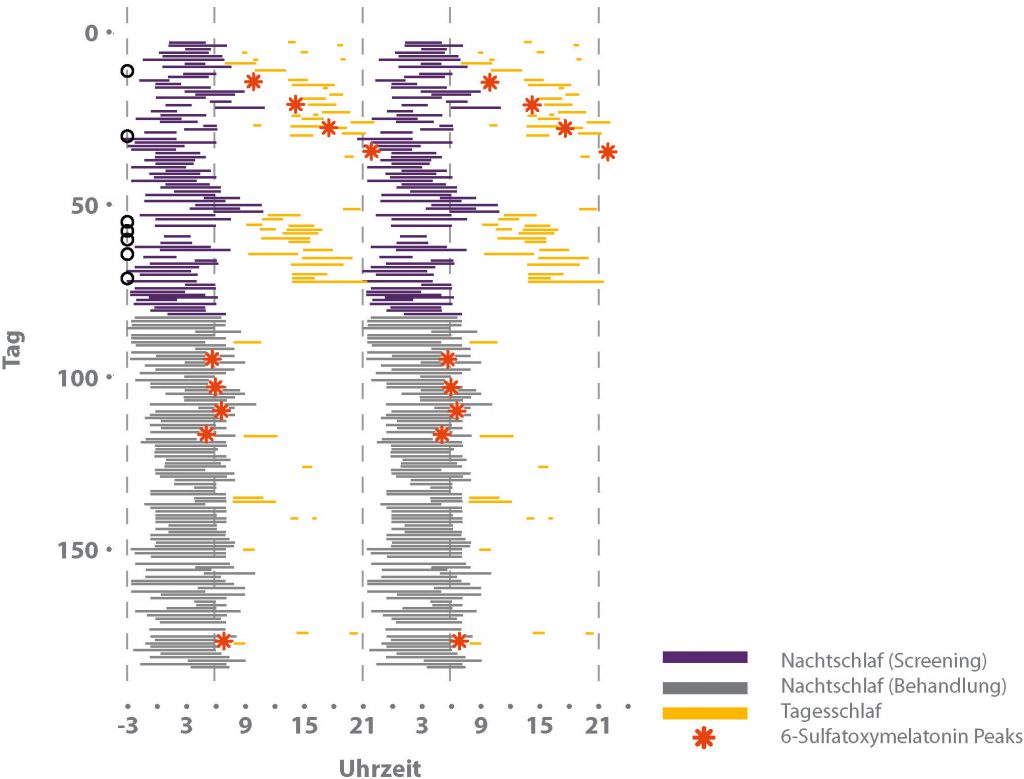
Abbildung 3: Schlafmuster eines Non-24 Patienten vor und nach der erfolgreichen Synchronisierung mit dem 24-Stundentag durch HETLIOZ®3
Die 6-Sulfatoxymelatonin-Peaks zeigen die Phase der biologischen Nacht an. Die fortlaufenden Verschiebungen während der Screening-Periode sind auf den freilaufenden Rhythmus der inneren Uhr dieses Patienten zurückzuführen.
Schon kurze Zeit nach Beginn der HETLIOZ®-Behandlung stabilisierte sich bei diesem Patienten der Peak in den Umgebungs-Nachtstunden und zeigt damit die erfolgreiche Synchronisierung der inneren Uhr mit dem 24-Stundentag an. Gleichzeitig normalisierte sich der Schlaf-Wach-Rhythmus. Die Synchronisierung bleibt im oben dargestellten Zeitraum unter kontinuierlicher HETLIOZ®-Behandlung bestehen.
RESET-Studie
Aufrechterhaltung der Synchronisierung und der Symptombesserung durch Weiterführung der HETLIOZ®-Therapie
Studiendesign3
Randomisierte, doppelblinde, placebokontrollierte Studie an völlig blinden Erwachsenen. Patienten mit Non-24 (n=20), die sich in einer Vorperiode unter HETLIOZ®-Therapie mit dem 24-Stundentag synchronisiert hatten (Periode τ (tau) 24,1 Stunden). Sie wurden randomisiert in zwei Gruppen zur Fortführung bzw. Absetzen der Behandlung mit HETLIOZ® über 8 Wochen aufgeteilt.
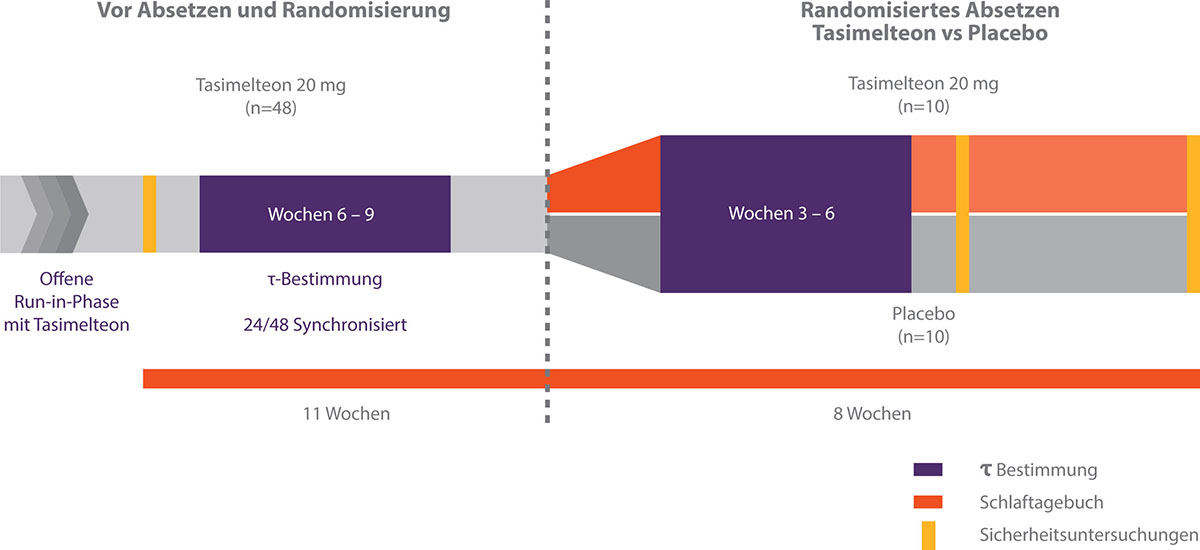
Abbildung 4: Design der RESET-Studie3
Ergebnisse der RESET-Studie:
90 % der Patienten in der Gruppe mit Weiterführung der HETLIOZ®-Therapie behielten die Synchronisierung mit dem 24-Stundentag, jedoch nur 20 % in der Placebo-Gruppe (p=0,0026).3
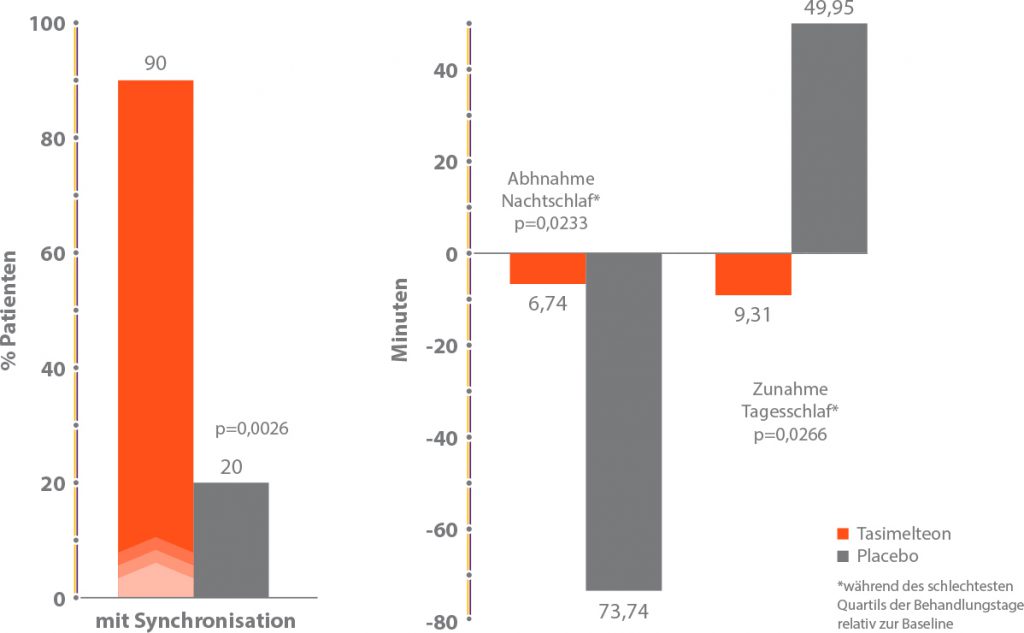
Abbildung 5: RESET-Studie: Veränderungen in der Schlafdauer nachts und tagsüber in den 25 % der symptomreichsten Nächte bzw. Tage unter Fortführung der HETLIOZ®-Therapie bzw. nach Switch auf Placebo3
- Patienten in der HETLIOZ®-Gruppe behielten ihre Nachtschlafdauer weitestgehend bei (-7 min), während in der auf Placebo veränderten Gruppe die Dauer des Nachtschlafs stark abnahm (-74 min) (p=0,0233).3
- Die Schlafdauer tagsüber nahm in der Placebo-Gruppe gegenüber dem Ausgangszustand um 50 min zu, während sich die HETLIOZ®-Patienten leicht weiter verbesserten (-9 min) (p= 0,0266).3
Die erfolgreiche Synchronisierung der biologischen Uhr kann eine mehrwöchige bis mehrmonatige Behandlung mit HETLIOZ® erfordern.
In Abbildung 6 werden erfolgreich mit HETLIOZ® synchronisierte Patienten aus der SET- und RESET-Studie in Abhängigkeit von der Behandlungsdauer zusammengefasst.7 Im ersten Monat nach Behandlungsbeginn waren 20 % der Patienten synchronisiert, nach 2 Monaten 37 % und nach 7 Monaten betrug die Erfolgsrate 59 %.7
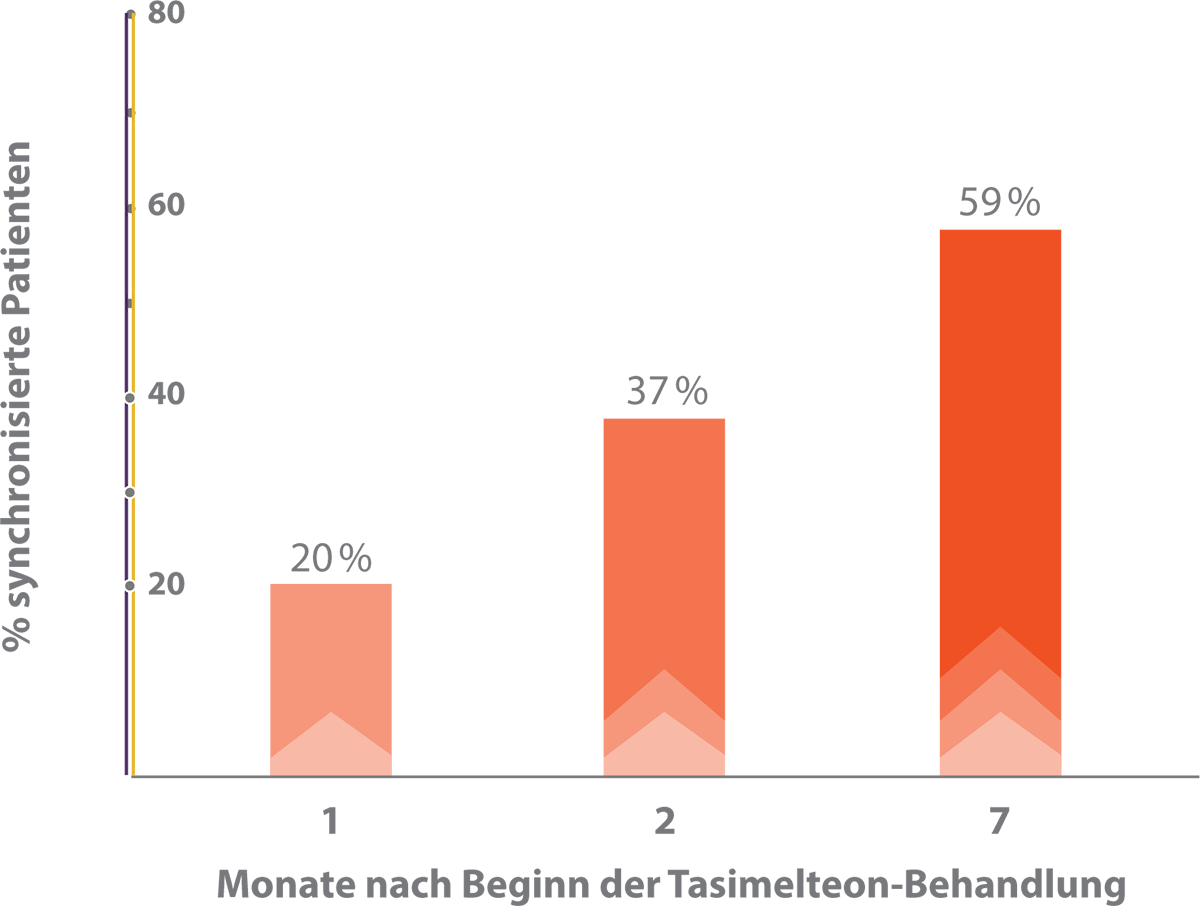
Abbildung 6: Die Synchronisierungsrate von Non-24-Patienten unter HETLIOZ®-Therapie nimmt mit steigender Behandlungsdauer zu (basierend auf den Ergebnissen der SET-/RESET-Studie)7
Eine schnelle Synchronisierung tritt wahrscheinlich dann ein, wenn die HETLIOZ®-Dosis bereits zu Behandlungsbeginn auf den optimalen Zeitpunkt während des zirkadianen Zyklus fällt, nämlich dann, wenn die innere Uhr gerade sensitiv gegenüber einem Zeitgeber-Impuls ist, d.h. am Synchronisationspunkt. Dies führt dann zu einer unmittelbaren Phasenverschiebung der inneren Uhr und zur Anpassung an den 24-Stundenrhythmus.8,9
Je weniger die endogene Periode den 24-Stundentag überschreitet, desto länger ist der zirkadiane Zyklus und desto unwahrscheinlicher ist es, den optimalen Synchronisationszeitpunkt gleich zu Behandlungsbeginn zu treffen, d.h. es wird eine längere Behandlungszeit benötigt bis die Synchronisierung erfolgen kann.8,9
Wie die RESET-Studie gezeigt hat, ist eine tägliche Behandlung mit HETLIOZ® erforderlich, um die Synchronisierung aufrecht zu erhalten.3
Referenzen:
1. Bjorvatn B & Pallesen S. A practical approach to circadian rhythm sleep disorders. Sleep Med Rev 2009;13:47-60.
2. Lockley S et al. Alertness, mood and performance rhythm disturbances associated with circadian sleep disorders in the blind. J Sleep Res 2008;17:207-216.
3. Lockley SW et al. Tasimelteon for non-24-hour sleep-wake disorder in totally blind people (SET and RESET): two multicentre, randomised, double-masked, placebo-controlled phase 3 trials. Lancet 2015;386:1754-1764.
4. Skene DJ et al. Correlation between urinary cortisol and 6-sulphatoxymelatonin rhythms in field studies of blind subjects. Clin Endocrinol 1999;50:715-719.
5. Lockley SW et al. Relationship between melatonin rhythms and visual loss in the blind. J Clin Endocrinol Metab 1997;82:3763-3770.
6. Vanda Pharmaceuticals Netherlands B.V. Fachinformation Hetlioz® (Stand Oktober 2022).
7. Zeitzer et al. Tasimelteon (HETLIOZ) synchronisiert die innere Uhr bei völlig blinden Personen mit dem Nicht-24-Stunden Schlaf-Wach-Syndrom (Non-24) und verbessert die Schlafparameter. DGSM Dezember 2016 (eingereicht).
8. Lewy AJ. Clinical applications of melatonin in circadian disorders. Dialogues Clin Neurosci. 2003;5:399-413.
9. Eastman C. Entraining the free-running circadian clocks of blind people. Lancet 2015 http://dx.doi.org/10.1016/S0140-6736(15)61451-9.
![HETLIOZ[R] (tasimelteon) capsules 20mg](../wp-content/themes/vanda/images/header-logo.jpg)
